ヘルスケアの未来を共に創る
ライセンサーが考えるライフサイエンスの未来
第3回 バッチライン(Batchline)
2025年12月、ビジネスエンジニアリング株式会社(B-EN-G)は、タイに本拠を置くBatchline社への資本参加(出資)を決定した。この決定の背景には、日本のライフサイエンス業界のお客様に、安心して運用できる次世代の製造インフラを提供するという強いコミットメントがある。
医薬品製造においては、データインテグリティ要件の厳格な順守と製造現場の効率向上は、往々にしてトレードオフの関係になりがちだ。しかし、B-EN-Gが戦略的パートナーとして選んだBatchlineの製造実行システム(MES)は、迅速に導入可能なソリューションでありながら、その両方を極めて高いレベルで実現している。
数あるソリューションの中から、なぜB-EN-GはBatchlineへの出資を決め、パートナーシップを選んだのか。Batchline社のGroup Executive DirectorであるDavid Margetts(デビッド・マーゲッツ)氏に、その革新的な設計思想と、両社のパートナーシップが日本の製薬市場にもたらす新たな価値について詳しく話を聞いた。(文中敬称略)
【聞き手】
ビジネスエンジニアリング株式会社 代表取締役社長 羽田 雅一
ビジネスエンジニアリング株式会社 取締役 ソリューション事業本部 副事業本部長 宮澤由美子
【ゲスト】
David Margetts(デビッド・マーゲッツ) 氏
Batchline Group Executive Director/医薬品製造DXおよびコンプライアンスのグローバルスペシャリスト。
製薬業界におけるデジタライゼーションおよび品質管理において25年以上のグローバルな経験を有す。
ISPE GAMP認定トレーナーを務め、CSV(コンピュータ化システムバリデーション)およびデータインテグリティの第一人者。長年にわたり、グローバル製薬企業に対してデジタライゼーションによるコンプライアンス強化と効率改善に関するアドバイザリーサービスを提供してきた。2004年にFactorytalkを共同設立し、2016年にはFactorytalk Groupの一員としてBatchline社を設立、業界の課題を解決する革新的なMESを開発している。
ミッションと背景
羽田:本日はありがとうございます。まず、Batchline設立の経緯と、製薬業界でどのような課題を解決しようとしているのか、改めてお聞かせください。
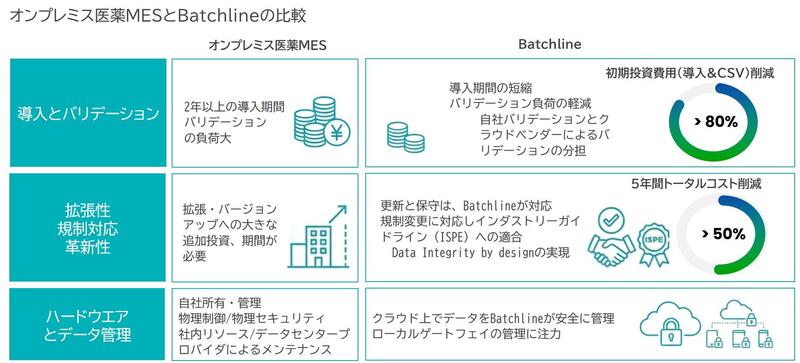
David Margetts氏(以下、DM):Batchlineは、製薬業界のソフトウェアIT、エンジニアリング、品質の最前線で数十年の経験を持つ専門家チームによって設立されました。解決したかった最大の課題は、従来のMES:製造実行システムが『高価で、導入が困難で、製造現場にとって不親切』である点です。多くの製薬企業が、複雑なシステム構成と膨大なバリデーション作業に苦労していました。そこで、私たちは、数年ではなく数週間で導入できる、『アジリティ』を核にしたソリューションを構築しました。私たちのミッションは、グローバルな規制基準(FDA、EMA、PICS/S)への準拠を確保しながら、驚くべきコスト効率を実現し、あらゆる規模の製薬企業がデジタライゼーションの恩恵を受けられるようにすることです。
これまで、製薬MESの導入には3つの高い障壁がありました。数億円規模の高額な投資コスト、数年に及ぶ導入の困難さ、そして膨大な専門作業と文書化を伴うバリデーション作業です。Batchlineは、これらの弱点を克服するために、アジリティと導入の容易さを設計思想の中核に据えました。数年ではなく数週間での導入を目指し、「Quality by Design」アプローチにより設計段階からコンプライアンスを組み込むことで、従来のMESの常識に挑戦しています。
B-EN-Gとのパートナーシップおよび出資の意義

羽田:B-EN-Gとのパートナーシップと今回の出資決定は、Batchlineにとってどのような戦略的意義を持つのでしょうか。
DM:B-EN-Gは、日本のライフサイエンス業界において極めて深い専門知識と確かな信頼を獲得しているパートナーです。今回の出資は、私たちの技術が日本の厳格な品質基準を満たしていることの力強い裏付けとなります。
DM:Batchlineのモダンで直感的なクラウド技術と、B-EN-Gが長年培ってきた医薬品製造に特化した導入・サポート能力を組み合わせることで、日本のお客様に最高レベルのコンプライアンスと安心を同時に提供することができます。これは、次世代の医薬品製造ソリューションをアジアから世界に発信するための重要な第一歩です。
ソリューションの核心:データインテグリティとコンプライアンス
宮澤:医薬品製造において、データインテグリティは避けて通れないテーマです。具体的に、BatchlineのMESは規制遵守(FDA 21 CFR Part 11、EMA、ISOなど)と現場の利便性をどのように両立させているのでしょうか。
DM:私たちはデータインテグリティを単なるチェックリスト項目としてではなく、システム設計・開発思想そのものの一部として捉えています。BatchlineはALCOA+(Attributable、Legible、Contemporaneous、Original、Accurate + Complete、Consistent、Enduring、Available)の原則を考慮したシステム機能を中心に構築されているため、お客様は設計によってALCOA+を確保でき、ソリューションを使用するだけで対応できます。
BatchlineのMESはFDA 21 CFR Part 11およびEU GMP Annex 11に完全準拠しており、堅牢な監査証跡、電子署名、アクセス制御を標準機能として備えています。
堅牢なデータインテグリティを確保した後の最大のメリットの一つが、Review by Exceptionの実現です。人が全工程の記録や大量の文書を目視確認するのではなく、システムが逸脱(例外)のみを即座に抽出することで、品質保証担当者の負担を大幅に軽減しながら、出荷判定までのスピードを加速します。
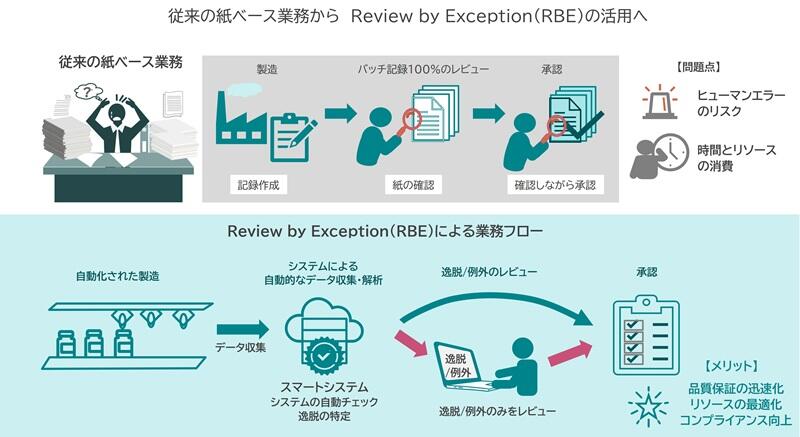
DM:さらに、すべての規制対象製造業者にサービスを提供するというミッションのもと、製造現場の利便性が損なわれないよう、ペーパーレス化の容易さに徹底的にこだわりました。例えば、モバイルデバイスでの直感的な操作とリアルタイムのエラー検出機能により、予期せぬ問題が発生した場合でも、オペレーターは自然に正しい手順に従うことができます。その結果、データと記録のコンプライアンス維持はデジタルチェックとガイダンスによって達成され、人的な時間とエラーを大幅に削減します。
グローバル展開とローカライゼーション

宮澤:タイを拠点としながらグローバルに展開されていますね。南北アメリカ、欧州、東南アジア、日本などの市場における「製造DX」の現状をどのようにご覧になっていますか。
DM:製造DXはグローバルに加速していますが、課題は地域によって異なります。欧米ではデジタライゼーションがコモディティ化しつつあり、企業はよりシンプルで低コストのツールを求めており、紙運用が持続可能でないことはすでに十分理解しています。東南アジアでは導入予算やITリテラシーにギャップがあり、一般的に変化を受け入れるのが遅い傾向にあります。そして日本は、極めて高い品質要件、既存の手順との緊密な適合、混乱を避けるための慎重な展開が特徴です。

DM:Batchlineのアプローチには、柔軟な多言語サポート、クラウドネイティブなスケーラビリティ、お客様の既存システムとの接続性、そしてグローバル標準の導入モデルとベストプラクティスバリデーションの提供が含まれます。高価なオンプレミスサーバーを必要とせず、各地域の言語やビジネス慣行に迅速に構成を適応させることができます。私たちの強みは、タイから世界中のあらゆる場所に、地域の状況に適応した最高の「グローバル品質」の製造ソリューションを提供できることです。
規制などに対応するために、どの企業も紙、あるいは簡易的なバッチレコードをベースとしていたやり方からMESへの「移行段階」を経ることになります。それは簡単なことではなく、コンサルティングサービスを必要とするでしょう。弊社としてのサービス提供という観点で考えるとそこが大事です。
将来ビジョン
宮澤:BatchlineとB-EN-Gのパートナーシップを通じて、5年後、10年後にグローバルな医薬品製造の姿がどのように変わるとお考えですか。
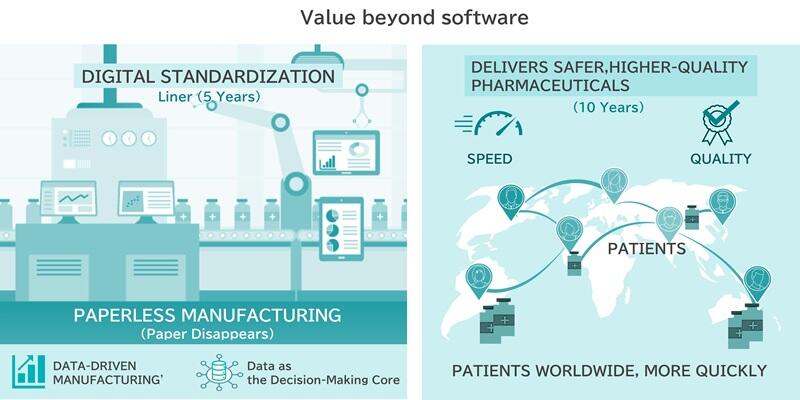
DM:私たちのパートナーシップは単なるソフトウェア提供にとどまりません。BatchlineとB-EN-Gの両社は、私たちのソフトウェアが現在のビジネスプロセスをデジタル化するだけでなく、医薬品製造がプロセス最適化のための適応型・予測型分析へと移行することを支援する未来を目指しています。5年後には、製造現場から「紙」がなくなるだけでなく、データが意思決定の核となる「データドリブン製造」が標準化されているでしょう。10年後には、B-EN-Gとともに構築したこのプラットフォームが、品質を継続的かつリアルタイムで保証し、サプライチェーン全体を可視化し、最終的には世界中の患者により安全で高品質な医薬品へのアクセスを届けることに貢献する重要なインフラになると確信しています。
おわりに:20年来の信頼から生まれた「共創」
インタビューの最後に、Batchline Group Executive DirectorのDavid Margetts氏はB-EN-Gとの特別な関係について語りました。
B-EN-Gは、私が20年間知り、一緒に仕事をしてきた会社です。私は常に、彼らの技術力、B-EN-Gの人々の誠実さ、そしてこれらの極めて重要で専門的な分野で達成された確かな実績とお客様の成功に深く感銘を受けてきました。
私たちはB-EN-GとともにBatchlineのコアチームを拡大し、このエキサイティングな旅を皆様と共有できることを大変嬉しく思います。
— David Margetts
20年にわたる重要な経験、専門家としての敬意と信頼に基づいているからこそ、BatchlineとB-EN-Gのパートナーシップは、日本の製薬業界に真の変革をもたらすという確信に満ちています。
企業プロフィール
Batchline は Factorytalk グループの一員です。 世界中で20年にわたり、GxPソリューションの提供とコンサルティングを行っています。
経営陣:
・David Margetts: Group Executive Director
・David Holt: Group Executive Director
・Orchun Thakral: Head of customer success
・Neil Wetherall: Managing Director of BatchLine UK
特徴:
・GxPデジタル化における公認のエキスパート
・拠点展開:本社: タイ(バンコク) 欧州オフィス: 英国(マンチェスター)
・ISO 9001:2015 認証取得済み
・ISPE GAMPの主要メンバーであり、業界ガイダンス出版物への寄稿も実施
ISPE業界活動:
・ISPE Good Practice Guide: Validation 4.0が、2025/06に発行されました。David Margettsは、Coリードとして活動しました。
https://ispe.org/publications/guidance-documents/good-practice-guide-validation-40
・ISPE GAMP Good Practice Guide: GxP Process Control Systems 3rd Edition.が2026/3に発行されました。David margettsはCoreメンバーとして活動しました。
https://ispe.org/publications/guidance-documents/gamp-good-practice-guide-gxp-process-control-systems-3rd-edition








